Cinética de degradación de vitamina C y vida útil de naranja (Citrus sinensis) conservado a diferentes temperaturas de almacenamiento
Kinetics of vitamin C degradation and shelf life of orange (Citrus sinensis) preserved at different storage temperatures
Antonio Otárola Gamarraa; Wuelber Joel Torres Suareza; Fortunato Candelario Ponce Rosasa;
Silvia María Murillo Bacaa; Hugo Rómulo Buendía Poncea; José Hernán Rodríguez Huataya;
Raque Estela Rosales Díaza, *
a Facultad de Ciencias Agropecuarias, Universidad Nacional Daniel Alcides Carrión. Av. Daniel Alomias Robles s/n, Ciudad Universitaria, Chanchamayo, Junín, Perú.
* Autor corresponsal: Antonio Otárola Gamarra [ aotarolaga@undac.edu.pe | http://orcid.org/0000-0003-3714-4027 ]
Wuelber Joel Torres Suarez [ https://orcid.org/0000-0002-8023-1890 ]
Fortunato Candelario Ponce Rosas [ https://orcid.org/0000-0003-0579-7226 ]
Silvia María Murillo Baca [ http://orcid.org/0000-0003-2403-2157 ]
Hugo Rómulo Buendía Ponce [ http://orcid.org/0000-0002-5289-5200 ]
José Hernán Rodríguez Huatay [ https://orcid.org/0000-0002-9120-0037 ]
Raquel Estela Rosales Díaz [ https://orcid.org/0009-0008-2063-7080 ]
Resumen
Esta investigación tuvo el propósito determinar el efecto de la temperatura de almacenamiento, en la cinética de degradación de la vitamina C y vida útil de la naranja Valencia (Citrus sinensis), en estado natural; almacenados por 15 días a tres rangos de temperatura, T1: (8 a 12) °C, T2: (13 a 19) °C y T3: (20 a 27) °C. Se evaluaron factores fisicoquímicos, color y de cinética de degradación: constante de degradación (k), Tiempo de reducción decimal (D), coeficiente de velocidad de reducción (Q10), energía de activación (Ea) y vida útil media. Los resultados indican pérdida de vitamina C en los tratamientos de: 74.902 mg/100 g, hasta (T1: 64,32; T2: 56,03 y T3: 46,60); estableciendo parámetros cinéticos de K1: 0,0219; K2: 0,0404 y K3: 0,0690, D1: 45,558; D2: 24,752 y D3:14,480, Q10: 2,359 y Ea: 13,589 kcal/mol. Existiendo efecto directo de la velocidad de degradación con las características fisicoquímicos, el color y temperaturas de almacenamiento; vida útil media para (T1: 31, T2: 17 y T3: 10) días. Entonces a menor velocidad de degradación, menos pérdida de vitamina C, mayor tiempo de vida útil de las naranjas.
Palabras clave: Vitamina C; cinética; degradación; naranja Valencia; almacenamiento.
Abstract
This research had the purpose of determining the effect of storage temperature on the kinetics of degradation of vitamin C and shelf life of Valencia orange (Citrus sinensis), in its natural state; stored for 15 days at three temperature ranges, T1: (8 to 12) °C, T2: (13 to 19) °C and T3: (20 to 27) °C. Physicochemical, color and degradation kinetic factors were evaluated: degradation constant (k), decimal reduction time (D), reduction rate coefficient (Q10), activation energy (Ea) and average useful life. The results indicate loss of vitamin C in the treatments of 74,902 mg/100 g, up to (T1: 64,32; T2: 56,03 and T3: 46,60); establishing kinetic parameters of K1: 0,0219; K2: 0,0404 and K3: 0,0690, D1: 45,558; D2: 24,752 and D3: 14,480, Q10: 2,359 and Ea: 13.589 kcal/mol. There is a direct effect of the degradation speed with the physicochemical characteristics, color and storage temperatures; average useful life for (T1: 31, T2: 17 and T3: 10) days. So, the lower the rate of degradation, the less loss of vitamin C, the longer the useful life of the oranges.
Keywords: Vitamin C; kinetics; degradation; Valencia orange; storage.
- Introducción
El cultivo de naranjas en la Selva Central del Perú involucra a muchos agricultores, después del café es el que más mano de obra requiere (Selva Industrial S.A., 2023); el año 2022 Chanchamayo cultivo 7309 ha, siendo su comercialización mayormente al granel en mercados de Lima y la región (Broco & Valderrama, 2010). Esta actividad se realiza sin un manejo adecuado, a temperaturas ambientales del momento en menor grado en comercios como supermercados, en pequeña cantidad va dirigido al comercio exterior y 14% va al mercado industrial, para jugos concentrados (Ruiz et al., 2024).
La vitamina C es esencial para el desarrollo normal del ser humano; sin embargo, el organismo humano no puede producir, por lo que se debe ingerir constantemente (Barca Innovation Hub, 2022). La vitamina C debe ser consumido en cantidades adecuadas por el ser humano, puesto que esta vitamina permite la acción de muchos minerales y otras vitaminas en el funcionamiento adecuado del organismo humano; como lo afirman Ali et al. (2024), el consumo de vitamina C favorece a la salud porque refuerza a absorber la tiamina, riboflavina, ácido pantoténico, biotina, ácido fólico, vitamina B12, vitamina E y vitamina A. La vitamina C ayuda en la absorción del Fe, en la reparación de los tejidos dañados, participa en la producción y activación de numerosas sustancias químicas de nuestro cuerpo. Giannakourou & Taoukis (2021) mencionan que se debe ingerir en alimentos mínimo 80 mg de vitamina por día. Rothan (2020) y Fenech (2019) dicen que el consumo de cítricos es importante para satisfacer la necesidad diaria de vitamina C.
La naranja brinda beneficio fortificante de vitamina C y fibra dietética que proporciona cada ración de zumo, motivo por el cual la población consume en gran parte (Saucedo & Torpoco, 2018), la vitamina C es sensible a la acción del calor (Ordoñez et al., 2013), como compuesto bioactivo se altera fácilmente por la acción de la temperatura, la luz, los cambios de pH y los iones metálicos. Asimismo, Quin et al. (2019) afirman que la degradación de este antioxidante funcional continúa durante el periodo de almacenamiento, por acción de la luz y temperatura se oxidan. Infobae (2024) y Lima et al. (2019), afirman que la naranja aporta al organismo gran cantidad de Vitamina C. El consumo de una naranja cubre las necesidades diarias de vitamina C, ya que contiene varios tipos de vitaminas, tales como el betacaroteno, provitamina A, vitamina B1, B2 y B9 (ácido fólico). Castillo (2019) menciona que la fibra soluble que posee facilita el movimiento intestinal para la correcta digestión y desarrollo de bacterias probióticas en el intestino. El ácido cítrico que abunda en la naranja potencia la acción de la vitamina C, favorece la asimilación del calcio, y facilita la expulsión de algunas toxinas del organismo como el ácido úrico (Pozo et al., 2020).
La mayor o menor vida útil del producto va a depender de la naturaleza del producto en sí, pero también de otros factores de manipulación (Murillo et al., 2022), los procesos de higiene y de conservación a los que se someta, condiciones de almacenamiento como temperatura, humedad, envasado, etc. Cabanillas & Aurora (2020) estable-cen que existe mayor sensibilidad de los parámetros cinéticos de degradación de vitamina C y color a mayor temperatura de exposición.
Por lo que es importante conocer la cinética de degradación de la vitamina C y su relación con los demás factores fisicoquímicos, almacenando a diferentes rangos de temperatura, calcular su vida útil en base al contenido de vitamina C. Así el objetivo de este estudio fue determinar el efecto de la temperatura de almacenamiento en la cinética de vitamina C y vida útil en frutos de naranja producida en Chanchamayo, Perú.
- Metodología
Naranjas variedad Valencia fueron cosechadas del Fundo La Esperanza, distrito de Perene, provincia de Chanchamayo, región Junín, Perú. Se cosecharon en estado de madurez fisiológica óptima, de color verde amarillo pintón (NTP. 2003.110, 2009; ICONTEC; 2013); las naranjas fueron lavadas con abundante agua potable, secados al ambiente, dispuestos 15 kg por tratamiento, almacenados a rango de tempe-ratura T1 de 8 °C a 12 °C (refrigeración), T2 de 13 °C a 19 °C y T3 de 19 °C a 27 °C (ambiente); por tiempo de 15 días (Tabla 1). Para los diversos análisis cada 48 horas, se tomaron muestras por triplicado al azar, pelados, cortados y exprimidos.
Tabla 1
Distribución de tratamientos
Tratamiento | Temperatura* | N° de controles | Tiempo* |
T1 | 8 a 12 °C | 8 | 15 días |
T2 | 13 a 19 °C | 8 | 15 días |
T3 | 20 – 27 °C (ambiente) | 8 | 15 días |
* Condiciones de almacenamiento
Días de control: 1, 3, 5, 7, 9, 11, 13, 15
Repeticiones: 3.
Análisis fisicoquímicos y color
Peso: se dispusieron 10 unidades de naranja enumerados, pesados en cada control, con balanza de precisión Henkel.
Sólidos solubles: método refractométrico a 20 °C (AOAC 932.12) utilizando refractómetro Hanna.
pH: método potenciométrico (AOAC 981.12) utilizando Potenciómetro MILWAUKEE, modelo MA871.
Acidez titulable: método de titulación (AOAC 942.15), expresado mg de ácido cítrico/100 g.
Índice de madurez: utilizando la relación sólidos solubles/acidez titulable.
Índice de color: mediante tabla (ICONTEC; 2013).
Contenido de vitamina C y parámetros cinéticos de degradación de la vitamina C
Concentración de vitamina C: se determinó utilizando el método espectrofotométrico, método oficial de la AOAC 967.21 con 2,6-dicloroindofenol (2,6 DFIF) (AOAC, 1995), expresados en mg ácido ascórbico/ 100 g muestra. Refractómetro Unico Spectrophotometer, modelo 1205E S/N WU18061805011; agitador magnético VELP Scientifica, modelo F20500011 S/N 500210.
Parámetros cinéticos: se calcularon empleando las siguientes ecuaciones.
Modelo cinético para orden cero:
[A]= [Ao] ± kt
Modelo cinético para orden uno:
[A]= [Ao] ± ekt
Donde [𝐴o] es la concentración inicial del atributo medido; [𝐴] la concentración del atributo medido a un tiempo 𝑡; k es una velocidad constante de reacción expresada en min-1; t es el tiempo en minutos.
Determinación de la constante K:
K = K0 exp-Ea/RT
Donde k es la constante de velocidad de reacción
𝑘0 es el factor pre- exponencial; -Ea es la energía de activación en kcal/mol; 𝑅 es la constante universal de los gases (1,9872 cal/K mol) o (8,3145 J/K mol); T es la temperatura absoluta en grados kelvin (K).
Cambio de la constante de velocidad de una reacción al aumentar la temperatura en 10 °C:
Q10 = [K2/K1]10/T2 – T1
Vida útil al 50 % de concentración de vitamina C:
T01/2 = ln (10)
𝑘
- Resultados y discusión
3.1. Caracterización fisicoquímica de la naranja
Durante el almacenamiento, el tratamiento T1: de 8 a 12 °C, pierde 9,75% de peso, sin embargo, el T2: de 13 a 19 °C pierde 7,20%, el T3: de 20 a 27 °C pierde 14,87% de peso (Figura 1), incluso presenta ligero perdida de humedad en la cáscara, valores superiores a lo hallado por Lord et al. (2016) almace-nados a 9 °C 7, 4% a 25 °C 10,3%, con recubrimiento de CMC. Rodríguez et al. (2001) determino pérdida de 2,3% almacenado a 2 °C y recubierto con parafina; Zacarias (2023) reporta perdida de 1,9% almacenado a 2 °C, recubierto con gel. Villares et al. (2024) determinaron pérdida de 47,8% a 26 °C por 10 días; Yajahuanca (2021) reporta pérdida de 9,81% en una semana de almacenamiento a T° de 14 a 18 °C. Demuestra que la temperatura de almacenamiento incide directamente en la conservación del peso de las naranjas.
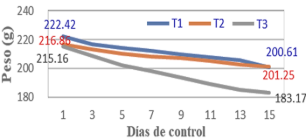
Figura 1. Tendencia de los pesos de las naranjas durante el almacenamiento. Peso promedio de 10 unidades de naranjas, pesados individualmente.
Los sólidos solubles inicial fueron de 10,93 y 11,03 °Brix, la variación durante el almacenamiento es mínimo 0,3 Brix, esto es porque la concentración de azucares es alto, comparado con lo reportado por Molina & Montesdeoca (2014) de 7,7 a 8,7 °Brix; Murillo et al. (2022) 10,0 °Brix, asimismo la NTP. 2003.110 (2009) indica 10 °Brix, para jugo de naranjas; Ledezma (2013) 9,0 °Brix inicial y una variabilidad hasta 14 °Brix almacenado a temperatura ambiente de 22 a 25 °C por 14 días; Villares et al. (2024) de 8,4 °Brix.
De lo reportado en Tabla 2 la variabilidad es notorio, para T1 de 2,33 a 3,50; T2 de 2,50 3,37 y T3 de 2,33 a 3,20, siendo la tendencia similar para los tres tratamientos y guarda una relación directa con la acidez y contenido de vitamina C. inferior a lo determinado por Murillo et al. (2022) de 3,20 a 3,55; Lord et al. (2016) 2.0 a 2.1; Aucayauri (2011) 3,4; Vidal (2017) 3,47 de pH. García (2012) menciona que las naranjas de mejor calidad tienen pH de 2,0 a 2,10. Giannakourou & Taoukis (2021) afirman que el pH entre 2 a 4 es el conserva mejor la vitamina C en la naranja.
Tabla 2
pH de las naranjas durante el almacenamiento
Días de control | T1 | T2 | T3 |
1 | 2,33+0,0001 | 2,50+0,0052 | 2,33+0,0577 |
3 | 2,61+0,0001 | 2,65+0,0058 | 2,67+0,0058 |
5 | 2,66+0,0001 | 2,64+0,0058 | 2,70+0,0057 |
7 | 2,68+0,0000 | 2,79+0,0058 | 2,93+0,0577 |
9 | 2,80+0,0000 | 2,86+0,0058 | 2,95+0,0100 |
11 | 3,06+0,0022 | 2,92+0,0693 | 3,10+0,1000 |
13 | 3,17+0,0022 | 2,89+0,0115 | 3,13+0,0577 |
15 | 3,50+0,0000 | 3,37+0,0577 | 3,20+0,1000 |
En la Tabla 3 se evidencia la acidez expresado en mg de ácido cítrico, así la variación existe para T1 de 0,5544 a 0,4664; T2 de 0,5544 a 0,4620 y de T3 de 0,5544 a 0,4400; valores menores a lo reportado por Vidal (2017) de 1,25 a 1,34; Aucayauri (2011) 0,576; Molina & Montesdeoca (2014) de 2,76 a 1,82 en 2 semanas de almacenamiento en frio y con cobertura; Murillo et al. (2022) expresa variabilidad en seis horas de 0,429 a 0,336; Bautista (2023) de 0,19 a 0,53; asimismo, la NTP 011.023 (2014) establece como mínimo 0,50 y máximo de 1,5; para naranjas de buena calidad, coincide con Gao et al. (2019), este otro factor es importante para la conservación de los alimentos.
Tabla 3
Acidez titulable de la naranja durante el almacenamiento
Días de control | T1 | T2 | T3 |
1 | 0,5544 | 0,5544 | 0,5544 |
3 | 0,5280 | 0,5236 | 0,5192 |
5 | 0,5192 | 0,5148 | 0,5104 |
7 | 0,5104 | 0,5060 | 0,4664 |
9 | 0,5016 | 0,5016 | 0,4576 |
11 | 0,4840 | 0,4884 | 0,4488 |
13 | 0,4752 | 0,4752 | 0,4444 |
15 | 0,4664 | 0,4620 | 0,4400 |
Inicialmente el índice de madurez (IM) es igual para los tres tratamientos 19,90; siendo la variabilidad para T1 a 23,80; T2 a 24,24 y T3 a 19,90; son valores altos en relación a otras investigaciones. NTP 011.023 (2014) considera mínimo 16,00 para una naranja de buena calidad. La empresa Yara Perú (2024), alude que para exportación las naranjas deben tener un mínimo de 14,00 a 16,00 de IM, que en el mercado de EE.UU. aprecian con valores de hasta 23,00. Molina & Montesdeoca (2014), hallaron de IM de 2,65 a 4,75; Lord et al. (2016) de 2,7 a 5,2; Pérez et al. (2020) de 6,80 a 7,20; Vidal (2017) indican valor de 9,60, valor relativamente apreciable; Aucayauri (2011) menciona que el IM de 16,96. en este factor inciden mucho el clima, altitud del cultivo (1200 msnm, en nuestro caso), asimismo el índice de madurez es alto por concentración alta de solidos totales y una acidez real menor a 0,5; y guarda relación con la concentración de vitamina C.
3.2. Color
En la Figura 2 los datos recogidos de acuerdo a la tabla de color para naranja Valencia de 0 a 6. ICONTEC (2013) recomienda hacer la cosecha en el estadio 3, donde existe equilibrio entre los sólidos solubles y acidez de la fruta; la variabilidad del índice de color (IC), iniciando de 3,0 para todos los tratamientos, presenta una variación para T1 de 3,35; T2 de 4,67 y T3 de 4,80; Filoteo et al. (2023) indican que a 30 días de almacenamiento a 16 °C, el IC fue el equivalente a 4,0; Jiménez et al. (2024) de 3,0 a 3,5 a 6 °C en 4 semanas; Yajahuanca (2021) de 3,5 a 3,6; almacenado por 2 semanas, recubierto con bicarbonato de sodio a temperatura de 14 a18 °C. Velázquez (2014) menciona que el cambio ligero en el color de los frutos es por la disminución del metabolismo, ya que esta actividad es dependiente de las temperaturas de almacenamiento, a menor temperatura, menor actividad metabólica, por lo tanto, menos cambios bioquímicos, que coincide con Arilla et al. (2022), respecto al cambio de color por estas causas; Zacarias et al. (2022) y Rodrigo et al. (2019) afirman que los carotenoides específicos como el α-caroteno, el β-caroteno y la β-criptoxantina son los principales componentes del desarrollo del color de los cítricos.
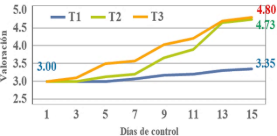
Figura 2. Variación del color de la naranja durante el almacenamiento.
3.3. Vitamina C de la naranja durante el almacenamiento
Los datos obtenidos durante el almacenamiento (Tabla 4), indica que la cantidad inicial 74,902 mg de ácido ascórbico / 100 g de muestra, existe mayor pérdida en el tratamiento T3 a 46,607, con Índice de Retención (IR) de 62,22%; T2 a 56,039, con IR de 74,81% y T1 a 64,320 con IR de 85,87%. El contenido inicial es similar a lo reportado por Murillo et al. (2022) (74,034 mg/100 g), Aucayauri (2011) (76,00 mg/100 g) y Akyildiz et al. (2021) (68,5 mg /100 g); sin embargo, Calderón (2007) obtuvo una cantidad mayor (94,253 mg/100 g), en contraste Vidal (2017) una cantidad menor (43,809 mg/100 g). Nakilcioğlu-Taş & Ötleş (2020) reportan pérdida de 14,73% de vitamina C en jugo almacenado a 25 °C; El-Naby et al. (2020) indican pérdidas de 16,5% almacenados al medio ambiente, en 6 días. El comportamiento de contenido de vitamina C es dependiente de la temperatura de almacenamiento, las frutas y los zumos en general pierden vitamina C durante el almacenamiento también por factores como la exposición a la luz, recubrimientos, conservantes añadidos, que coincide con Randhawa et al. (2020) y Quillimamani (2022). Ordoñez et al. (2013) determinaron una degradación de vitamina C en jugo de guayaba de 75,0 mg/100 g. Baltazari et al. (2020) afirman que la temperatura adecuada de almacenamiento de cítricos es de 5 °C a 20 °C. Cánova et al. (2020) indican que el requerimiento mínimo es de 80 mg de vitamina C por día. La temperatura de almacenamiento tiene efecto directo sobre el contenido de vitamina C, a mayor temperatura, mayor pérdida de vitamina C. Asimismo factores de manipulación en el transporte y condiciones de comercialización no adecuada, como la venta ambulatoria.
Tabla 4
Variación de la vitamina C (mg/100 g) de la naranja durante el almacenamiento
Días de control | T1 | T2 | T3 |
1 | 74,902 | 74,902 | 74,902 |
3 | 73,016 | 72,261 | 71,130 |
5 | 71,507 | 68,866 | 66,791 |
7 | 70,375 | 66,602 | 62,075 |
9 | 68,489 | 63,584 | 57,925 |
11 | 66,791 | 61,509 | 54,152 |
13 | 65,470 | 59,434 | 49,814 |
15 | 64,320 | 56,039 | 46,607 |
IR (%) | 85,872 | 74,816 | 62,223 |
IR: Índice de retención.
3.4. Parámetros cinéticos de la degradación de vitamina C
Orden de las reacciones. En las figuras 3 y 4 se muestra la determinación del orden de reacción de los tres tratamientos almacenados a diversos rangos de temperatura y se determinó el orden de reacción cinético de la vitamina C, para lo cual se utilizaron los datos obtenidos que se observan en los gráficos, de ello se considera lo más adecuado la cinética de orden 1 (n=1), puesto que los valores del coeficiente de determinación se encuentran cercanos a uno, por lo que se consideran un mejor ajuste lineal.
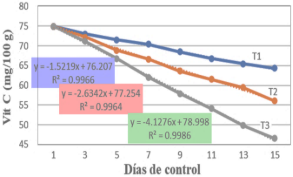
Figura 3. Cinética de degradación de la vitamina C en la naranja, reacción de orden 0.
Soceanu et al. (2021) y Quillimamani (2019) indican que la degradación de la vitamina C normalmente se ajusta a una cinética de orden cero o de primer orden, dependiendo de la variabilidad de temperaturas. Nakilcioğlu-Taş & Ötleş (2020), Giannakourou & Taoukis (2021), Iglesias-Carres et al. (2019), Murillo et al. (2022), Adenya & Atta-Eyison (2024), y Hernández et al. (2024) consideran adecuado el empleo del orden cinético de primer orden para medir la velocidad de degradación del jugo de naranja. Cabanillas & Aurora (2020) en pulpa de pitahaya indica que la degradación de la vitamina C según sus coeficientes de determinación R2 sugieren el modelo de primer orden, en misma tendencia. Riera & Gómez (2019) indican que el orden 1 se ajusta mejor para evaluar la degradación de la vitamina C.
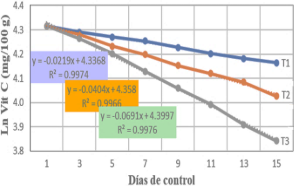
Figura 4. Cinética de degradación de la vitamina C en la naranja, reacción de orden 1.
Parámetros cinéticos para determinar la vida útil de las naranjas
La constante de velocidad de reacción (K) registra una concentración inicial de vitamina C igual para los 3 tratamientos, la velocidad de reacción esta dado para T1: 0,02195 h-1, T2: 0,04040 h-1 y T3: 0,06906 h-1, respectivamente (Tabla 5), se incrementa conforme aumenta la temperatura de almacenamiento, que coincide con lo descrito por Aucayauri (2011) y Murillo et al. (2022). Ellos encontraron un orden creciente de la velocidad de degradación de vitamina C conforme se incrementa la temperatura de conservación. Ramírez (2019) determinó para el tratamiento térmico de zumo de aguaymanto una velocidad de reacción de 0,0731, 0,0952 y 0,1244 h-1 para 60, 70 y 80 °C, respectiva-mente, evidenciándose un incremento conforme aumenta la temperatura. Cabanillas & Aurora (2020), en pulpa de pitahaya, encontraron la misma tendencia, a medida que la temperatura aumenta (75 a 90 °C) el parámetro cinético K pasó de 0,0557 a 0,1598 h-1. Riera & Gómez (2019) y Yin (2022) afirman que se incrementa la tasa de degradación de ácido ascórbico cuando el almacenamiento se realiza a altas temperaturas. Zamora (2019) determinó para jugo de arándano a 60, 70 y 80 °C valores de 0,0848, 0,9996 y 0,9998 h-1, respecti-vamente. Entonces, la velocidad de oxidación de vitamina C de las frutas aumenta conforme se incrementa la temperatura.
Tabla 5
Temperatura y constante de degradación para la determinación de la Ea en la ecuación de Arrhenius
Tratamiento | T° C | T°K | K | D: 1/T (hr) | Ln K | Q10=(K2/K1)10/t2-t1 |
T1 | 10 | 283,15 | 0,02195 | 45,55808 | -3,81917 | 2,3597 |
T2 | 16 | 289,15 | 0,04040 | 24,75247 | -3,20898 |
T3 | 24 | 297,15 | 0,06906 | 14,48016 | -2,67285 |
Los valores de D para T1: 45,5580 h; T2, 24,7524 h y T3: 14,4801 h, indican que se requiere esos tiempos para reducir un ciclo logaritmo, el contenido de vitamina C en la naranja almacenado en condiciones de los tratamientos establecidos, las temperaturas que están en la Tabla 6, son las que con mayor frecuencia se presentaron en cada rango de los tratamientos; como se observa a menor temperatura de almacenamiento menor es la velocidad de degradación, por lo tanto se requiere mayor tiempo para reducir un ciclo logarítmico la vitamina C en la naranja almacenada. Al respecto Widyastuti (2022) dice es el tiempo necesario para la reducción de un ciclo logarítmico la degradación, entonces a menor temperatura es más lenta la degradación, lo queda demostrado con los datos hallados en este estudio, donde el valor D dismi-nuye al aumentar la temperatura de almacena-miento. Ordoñez et al. (2013) determinaron para jugo de guayaba valor D de 2,88 a 1,55 min, para temperaturas de 75 y 95 °C, respectivamente; Quillimamani et al. (2022), para zumo de tumbo, a 60, 70 y 80 °C determinaron valores D de 162,17, 121,74 y 101,76 minutos; igual tendencia describe Leandro (2021) para pulpa pasteurizado de camu camu.
El valor de Q10 es 2,3597 (Tabla 6) para la vitamina C durante el almacenamiento por 15 días a tres rangos de temperatura, indicando que la velocidad de pérdida de esta vitamina en un equivalente a 2,3597 cuando la temperatura de almacenamiento cambia en 10 °C. Shafiur (2003) define el valor Q10 como el cambio que tiene lugar en la constante de velocidad de reacción como consecuencia de un cambio de temperatura de 10 °C. Al respecto Ordoñez et al. (2013) determinaron el valor Q10 de 1,35 para zumo de naranja pasteurizado a temperaturas de 75, 85 y 95 °C. Murillo et al. (2022) hallaron un valor Q10 de 0,833 para zumo de naranja en una variabilidad de temperatura de 8 °C a 27 °C. Leandro (2021) halló un valor Q10 de 1,55, durante la pasteurización de pulpa de camu camu a temperaturas de 70 a 90 °C. Barreto & Fierro (2021) para congelamiento de pulpa de camu camu a 0°C y -38 °C encontraron un valor de Q10 de 1,99. Cedeño et al. (2021), para néctar de durazno, un Q10 de 1,51 para variación de temperatura de 22 a 45 °C. El valor hallado en el presente estudio es propor-cional a lo que reportan los autores citados, por efecto de la variabilidad de las temperaturas y tiempo de almacenamiento. Estos valores indican la dependencia de la degradación del ácido ascórbico con la temperatura, por lo que almacenado a menores temperaturas se prolonga la vida útil de este producto.
La energía de activación (Ea) es la energía mínima necesaria para la activación de una reacción química o que una reacción se desarrolle y forme un campo activado. La Ea fue 13,5809 Kcal/mol (Tabla 6). Murillo et al. (2022), para el jugo de naranja, calcularon una Ea de 3,0778 Kcal/mol; de igual forma Aucayauri (2011) halló una Ea de 6,2975 kcal/mol para jugo de naranja pasteurizado de 70, 80 y 90 °C. Cabanillas (2020) en pulpa de pitahaya muestra una Ea de 70,4168 KJ/mol. La velocidad de degradación del ácido ascórbico respecto a la variación de la temperatura de almacenamiento puede apreciarse en la Figura 5. La vida útil en relación a contenido de vitamina C, Según datos reportados en Tabla 6, la degradación media de vitamina C en las naranjas almacenadas a T1 (8 a 12 °C), T2 (13 a 19 °C) y T3 (20 a 27 °C), presentan una vida útil en función al contenido de vitamina C al 50% de 32, 17 y 10 días, aparte de los 15 días de almacenamiento. Esto concuerda con Lu et al. (2019), quienes argumentan que una temperatura alta de almacenamiento provoca una menor vida útil de los cítricos. Igualmente, Burdiarto et al. (2024) mencio-nan que todos los genotipos de cítricos exhiben una disminución confirmada en los niveles de vitamina C a temperaturas altas de almacenamiento.
Tabla 6
Parámetros cinéticos de degradación de vitamina C de la naranja en almacenamiento y cálculo de la vida útil.
T° | Tratamiento | Co inicial (mg/100g) | t(1/2) vida media (Ln2/K) | Ea/R | Ea (kcal/mol) |
10 | T1 | 74,902 | 31,5842 | 6839,199 | 13,5809 |
16 | T2 | 74,902 | 17,1580 |
24 | T3 | 74,902 | 10,0376 |
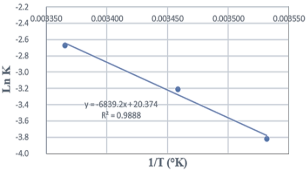
Figura 5. Modelo de Arrhenius de cinética de degradación de vitamina C de la naranja durante el almacenamiento.
- Conclusiones
La temperatura de almacenamiento tiene efecto directo en la cinética de degradación de la vitamina C y vida útil de la naranja Valencia, presentando un orden cinético de primer orden. Se encontró que existe relación directa de la velocidad de degradación con las temperaturas de almacenamiento, es decir, a menor temperatura de almacenamiento, menor velocidad de degradación, consecuentemente, menor pérdida de vitamina C. La vida útil de naranjas evaluadas es de 32, 17 y 10 días, luego de los 15 días de almacenamiento para los tratamientos T1 (8 a 12 °C), T2 (13 a 19 °C) y T3 (20 a 27 °C), respectivamente.
La cinética de la vitamina C almacenado a diferentes rangos de temperatura presenta valor D de 45,5580 h para T1, 24,7524 h para T2 y 14,4801 h para T3; valor de Q10 de 2,3597 y energía de activación 13,5809 Kcal/mol; que constituyen el desarrollo de la cinética de degradación de la vitamina C en las condiciones de los tratamientos evaluados.
Para profundizar en los procesos degradativos, se debería evaluar la actividad antioxidante del zumo de naranja, a diferentes condiciones de almacenamiento y su relación con la cinética de degradación.
Referencias bibliográficas
A.O.A.C. (2005). Official Method 967.21 Ascorbic Acid in Vitamin Preparations and Juices. 18.
A.O.A.C. (2007). Official Methods Analysis of AOAC International". 18th edition., Maryland. 932.12; 981.12; 942.15.
Adenya, E. & Ashiagbor, & Atta-Eyison, A. (2024). Determination of ascorbic acid levels in oranges under different storage conditions using Redox Iodometric method. World Journal of Advanced Research and Reviews, 22(1), 1169–1179. https://doi.org/10.30574/wjarr.2024.22.1.1165
Akyildiz, A., Mertoglu, T. S., & Agcam, E. (2021). Kinetic study for ascorbic acid degradation, hydroxymethylfurfural and furfural formations in orange juice. Journal of Food Composition and Analysis, 102, 103996. https://doi.org/10.1016/j.jfca.2021.103996
Ali, A., Riaz, S., Khalid, W., Fatima, M., Mubeen, U., Babar, Q., Manzoor, F. M., Khalid, M. Z., & Madilo, F. K. (2024). Potential of ascorbic acid in human health against different diseases: an updated narrative review. International Journal of Food Properties, 27(1), 493-515. https://doi.org/10.1080/10942912.2024.2327335
Andrade, R. D., Blanquicett, K., & Rangel, R. D. (2016). Efecto del pH, sólidos solubles y zumo adicionado sobre el color y la vitamina C de zumo de naranja agria cristalizado. Información Tecnológica, 27(6), 129–134. http://dx.doi.org/10.4067/S0718-07642016000600013
Arilla, E., García-Segovia, P., Martínez-Monzó, J. et al. (2021) Effect of Adding Resistant Maltodextrin to Pasteurized Orange Juice on Bioactive Compounds and Their Bioaccessibility. Foods, 10, 1198. https://doi.org/10.3390/foods10061198
Aucayauri, E. (2011). Estudio de la cinética de degradación térmica del ácido ascórbico durante la pasteurización del zumo de naranja Valencia (Citrus sinensis). (Tesis de pregrado grado, Universidad Nacional del Centro del Perú).
Baltazari, A., Mtui, H. D., Mwatawala, M. W., Chove, L. M., Msogoya, T., Samwel, J., & Subramanian, J. (2020). Effects of storage conditions, storage duration and post-harvest treatments on nutritional and sensory quality of orange (Citrus sinensis (L) Osbeck) fruits. Int. J. Fruit Sci., 20(4), 737–749. https://doi.org/10.1080/15538362.2019.1673278
Barca Innovation Hub (2022). The importance of vitamin C in the performance of a professional athlete. https://barcainnovationhub.fcbarcelona.com/es/blog/la-importancia-de-la-vitamina-c-en-el-rendimiento-de-un-deportista-profesional/
Barreto, L., & Rojas, N. (2021). Cinética de degradación del ácido ascórbico durante la conservación por refrigeración y congelación de la pulpa de camu camu (Myrciaria Dubia (H.B.K.) Mc Vaugh). (Tesis de pregrado, Universidad Nacional del Centro del Perú).
Bautista, Z. (2023). Efecto de la técnica postcosecha a temperatura ambiente para prolongar la vida útil de la naranja (Citrus Sinensis) de San Cristóbal, Galápagos. (Tesis de pregrado, Universidad Agraria del Ecuador).
Budiarto, R., Mubarok, S., Sholikin, M. M., Sari, D. N., Khalisha, A., Sari, S. L., Rahmat, B. P. N., Ujilestari, T., & Adli, D. N. (2024). Vitamin C variation in citrus in response to genotypes, storage temperatures, and storage times: A systematic review and meta-analysis. Heliyon, 10(8), e29125. https://doi.org/10.1016/j.heliyon.2024.e
Cabanillas, E., & Aurora, E. F. (2020). Estudio de la cinética de degradación de vitamina C y color de pulpa de pitahaya (Hylocereaus monacanthus) pasteurizada (Tesis de pregrado, Universidad Señor de Sipán).
Castillo-Velarde, R. E. (2019). Vitamina C en la salud y en la enfermedad. Revista de la Facultad de Medicina Humana, 19(4), 95-100. http://dx.doi.org/10.25176/RFMH.v19i4.2351
Cedeño, L., Díaz, R., Armijos, G., San Martín, D., & Porras, M. (2021). Degradación del ácido ascórbico en néctar de durazno enriquecido. Journal of science and research, 7(1), 53–65. https://doi.org/10.5281/zenodo.6505535
El-Naby, S. K., Baiea, M. H., Abdelkhalek, A., Amin, O. A. E., & Khalifa, R. (2020). Mitigation of heat stress effects using agricultural treatments on growth; yield and fruit quality of Washington navel orange trees grown in Egypt. Plant Archives, 20(2), 2128-2133.
Fenech, M., Amaya, I., Valpuesta, V., Botella, M. A. (2019). Vitamin C content in fruits: biosynthesis and regulation. Front. Plant Sci., 9, 9. https://doi.org/10.3389/fpls.2018.02006
Filoteo, J., Elizondo, J., Martinez, J., Barron, J., Díaz, A., Saldivar, V., Estudillo, J., & Rojas, R. (2023). Non-Invasive Optoelectronic System for Color-Change Detection in Oranges to Predict Ripening by Using Artificial Neural Networks. IEEE Photonics Journal, 15(5).
Gao, Y., Liu, Y., Kan, C., Chen, M., & Chen, J. (2019). Changes of peel color and fruit quality in navel orange fruits under different storage methods. Sci. Hortic., 256 https://doi.org/10.1016/j.scienta.2019.05.049
García, (2012). Evaluación de la maduración y calidad de la naranja (Citrus sinensis) bajo requerimiento de frio. (Tesis doctoral, Universidad Laica Eloy Alfaro de Manabí, Colombia).
Giannakourou, M. C., & Taoukis, P. S. (2021). Effect of Alternative Preservation Steps and Storage on Vitamin C Stability in Fruit and Vegetable Products: Critical Review and Kinetic Modelling Approaches. Foods, 10(11), 2630. https://doi.org/10.3390/foods10112630
Hernández, D., Salar, F., Garre, A., Fernandez, P., García, C., & Frias, J. (2024). Kinetic modelling of anthocyanins and vitamin C degradation in a maqui-citrus beverage during storage for different sweeteners and pasteurization treatments. LWT, 199. https://doi.org/10.1016/j.lwt.2024.116082
ICONTEC (2013). Norma Técnica colombiana: Naranja Valencia Especificaciones.
Iglesias-Carres, L., Mas-Capdevila, A., Bravo, FI. et al. (2019) Optimization of a polyphenol extraction method for sweet orange pulp (Citrus sinensis L.) to identify phenolic compounds consumed from sweet oranges. PloS ONE, 14, Article e0211267. https://doi.org/10.1371/journal.pone.0211267
Lima, A. C. D., Cecatti, C., Fidélix, M. P. et al. (2019). Effect of Daily Consumption of Orange Juice on the Levels of Blood Glucose, Lipids, and Gut Microbiota Metabolites: Controlled Clinical Trials. Journal of Medicinal Food, 22, 202–210. https://doi.org/10.1089/jmf.2018.0080
Loord, R., Mesias, F., Prado, A., Molina, A., & Montesdeoca, C. (2016). Evaluación postcosecha de naranjas almacenadas con agentes de recubrimiento. Revista ESPAMCIENCIA, 7(1), 59-65.
Lu, Q., Huang, N., Peng, Y., Zhu, C., & Pan, S. (2019). Peel oils from three citrus species: volatile constituents, antioxidant activities and related contributions of individual components. J. Food Sci. Technol., 56(10), 4492–4502. https://doi.org/10.1007/s13197-019-03937-w
Molina, A., & Montesdeoca, C. (2014). Evaluación postcosecha de naranjas (Citrus sinensis L.) almacenadas a temperatura ambiente y de refrigeración aplicando agentes de recubrimiento. (Tesis de pregrado, Escuela Superior Politécnica Agropecuaria de Manabí Manuel Félix López).
Murillo, S., Ponce, F., Otárola, A., Torres, W., & Buendía, H. (2022) Cinética de degradación de vitamina c en jugo de naranja (Citrus sinensis) envasado y conservado a diferentes temperaturas en condiciones de Chanchamayo. Manglar, 20(1), 15-21. https://doi.org/10.57188/manglar.2023.002
Nakilcioğlu-Taş, E., & Ötleş, S. (2020). Kinetic modelling of vitamin C losses in fresh citrus juices under different storage conditions. Annals of the Brazilian Academy of Sciences.
Normas Técnicas Peruanas. (2014) NTP 011.023: Cítricos. Mandarinas, tangelos, naranjas y toronjas. Requisitos. https://www.procitrus.org/img-apps/info-notas/infonotas-1600203821.pdf
Ordóñez, L., Ospina, M., & Rodríguez, D. (2013). Cinética de degradación térmica de vitamina C en frutos de guayaba (Psidium guajava L.). Revista Lasallista de Investigación, 10(2), 44-51.
Pérez, L., Robles, J., Pizarro, L., & Casimiro, E. (2020). Evaluación de pérdidas poscosecha de naranjas (Citrus sinensis) producidas en la selva central del Perú. Revista Iberoamericana de Tecnología Postcosecha, 21(2). 87–94.
Pozo, S., Ávila, J., Ruiz, E., Valero, T., & Varela, G. (2022). Valor Nutricional de las Naranjas y Clementinas. Fundación Española de la Nutrition. https://www.fen.org.es/storage/app/media/imgpublicaciones/432011819.pdf
Qin, X., Liu, J., Du, Y., Li, Y., Zheng, L., Chen, G., & Cao, Y. (2019) Different doses of vitamin C supplementation enhances the Th1 immune response to early Plasmodium yoelii 17XL infection in BALB/c mice. Int. Immunopharmacol., 70, 387–395. https://doi.org/10.1016/j.intimp.2019.02.031
Quillimamani, S., Chambi, A., & Coaquira, J. (2022). Evaluación de la cinetica de degradación térmica de la vitamina C en la pulpa de tumbo (Pasiflora mollisima b). Revista de Difusión cultural y científica de la Universidad La Salle en Bolivia, 24(24), 145-164.
Ramírez, B. (2019). Cinética de la degradación del ácido ascórbico durante la deshidratación del Aguaymanto (Physalis Peruviana I.). (Tesis de pregrado, Universidad Nacional del Callao).
Randhawa, M. A., Javed, M. S., Ahmad, Z., Amjad, A., Khan, A. A., Shah, F. -U. -H., Filza, F. (2020). Amassing of hydroxymethyl-furfural, 2-furfural and 5-methyl furfural in orange (Citrus reticulata) juice during storage. Food Sci. Technol., 40(2), 382–386. https://doi.org/10.1590/fst.41718
Riera, M., & Gómez, Y. (2019). Influencia de las condiciones de almacenamiento en la degradación de vitamina C. Publicaciones en ciencias y tecnologías, 13(2), 3-11. https://doi.org/10.13140/RG.2.2.29489.53600
Rodrigo, M. J, Lado, J., Alós, E., Alquézar, B., Dery, O., Hirschberg, J., et al. (2019). Un alelo mutante de la ɞ-caroteno isomerasa (Z-ISO) está asociado con la pigmentación amarilla del mutante de naranja dulce "Pinalate" y revela nuevos conocimientos sobre su papel en la carotenogénesis de la fruta. BMC Plant Biol., 19(1), 465. https://doi.org/10.1186/s12870-019-2078-2
Rothan, H. A., & Byrareddy, S. N. (2020). The epidemiology and pathogenesis of coronavirus disease (COVID-19) outbreak. J. Autoimmun, 109. https://doi.org/10.1016/j.jaut.2020.102433
Ruiz, W., Suarez, J., Vega, E., Maldonado, I., Santa Cruz, R., Pérez, R., Paredez, J., Rodríguez, F., & Suarez, E. (2024). Diagnóstico tecnológico del sector Citrícolas en Chanchamayo, Junín: Análisis de demanda. Editorial Fundación Ediciones Clio.
Saucedo, T., & Torpoco, L. (2018). Contenido de ácido ascórbico en zumo de naranja (Citrus sinensis) embotellado expendido de forma ambulatoria en relación al recién exprimido en Lima. (Tesis de pregrado, Universidad Notbert Wiener – Perú).
Selva Industrial S.A. (2023). La Naranja Peruana. Boletín informativo Naranja – junio 2023.
Soceanu, A., Matei, N., Dobrinas, S., & Popescu, V. (2021). Degradation kinetic modelling of ascorbic acid from orange juice. Proceedings, 70(1), 55. https://doi.org/10.3390/foods_2020-07693
Velázquez, M. (2014). Acondicionamiento y encerado para disminuir el estrés por frio en naranja. Tesis de maestría en ciencias, Colegio de postgraduados. Centro de Investigación en Química Aplicada, Montecillo, Texcoco, México).
Villares, J., Cobos, M., Vásquez, L., Sarmiento, R., Maita, F., Freire, C., Lascano, A., & Alvarado, J. (2024). Evaluación de parámetros de calidad de naranja (Citrus × sinensis) en tres estados de madurez. Bionatura Journal. https://bionaturajournal.com/files/2-BJN-2024.01.01.10.pdf
Widyastuti, R. A. D., Budiarto, R., Warganegara, H. A., Timotiwu, P. B., Listiana, I., & Yanfika, H. (2022). ‘Crystal’ guava fruit quality in response to altitude variation of growing location. Biodiversitas J. Biol. Divers. 23(3). https://doi.org/10.13057/biodiv/d230344
Yajahuanca, E. (2021). Efecto del empleo de conservantes químicos para cítricos en el tiempo de conservación post cosecha de la naranja Valencia (Citrus sinensis “Valencia”). (Tesis de pregrado, Universidad Nacional Mayor de San Marcos, Perú).
Yin, X., Chen, K., Cheng, H., Chen, X., Feng, S., Song, Y., & Liang, L. (2022). Chemical stability of ascorbic acid integrated into commercial products: A review on bioactivity and delivery technology. Antioxidants, 11(1), 153. https://doi.org/10.3390/antiox11010153
Zacarias, L. (2023). Daños por frío y otros desordenes postcosecha en frutos cítricos: sintomatología, factores implicados y estrategias para su control. https://www.seminarioprocitrus.org/ponencias/diamiercoles/5-LORENZO-ZACARIAS-IATA-ESPA%C3%91A.pdf
Zacarias-García, J., Cronje, P. J., Diretto, G., Zacarias, L., & Rodrigo, M. J. (2022). A comprehensive analysis of carotenoids metabolism in two redfleshed mutants of Navel and Valencia sweet oranges (Citrus sinensis). Front. Plant Sci., 13,1034204. https://doi.org/10.3389/fpls.2022.1034204